|
|
市場調査レポート
商品コード
2034858
生物製剤安全性試験の世界市場:オファリング別、試験タイプ別、用途別、エンドユーザー別、地域別 - 2031年までの予測Biologics Safety Testing Market by Product (Kits, Reagents, Instruments), Services, Test Type (Mycoplasma, Sterility, Endotoxin, Bioburden), Product & Services by Application (Vaccines, mAbs, CGT), End User, Competition, Region - Global Forecast to 2031 |
||||||
カスタマイズ可能
|
|||||||
| 生物製剤安全性試験の世界市場:オファリング別、試験タイプ別、用途別、エンドユーザー別、地域別 - 2031年までの予測 |
|
出版日: 2026年05月04日
発行: MarketsandMarkets
ページ情報: 英文 527 Pages
納期: 即納可能
|
概要
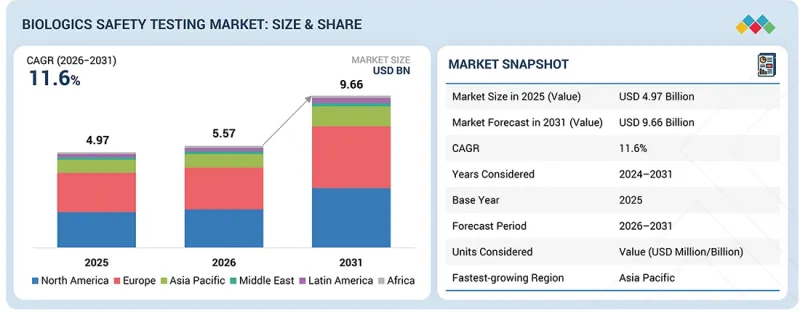
世界の生物製剤安全性試験の市場規模は、2026年の55億7,000万米ドルから、2031年までに96億6,000万米ドルに達すると推定されており、2026年から2031年の予測期間においてCAGR11.6%で成長すると見込まれています。
世界の生物製剤安全性試験市場は、生物製剤およびバイオシミラーのパイプラインの拡大、ならびに細胞・遺伝子治療やmRNA製品などの先進的な治療法の成長に支えられ、予測期間中に力強い成長を遂げると見込まれています。
| 調査範囲 | |
|---|---|
| 調査対象期間 | 2026年~2031年 |
| 基準年 | 2025年 |
| 予測期間 | 2026年~2031年 |
| 対象単位 | 金額(10億米ドル) |
| セグメント | オファリング別、試験タイプ別、用途別、エンドユーザー別、地域別 |
| 対象地域 | 北米、欧州、アジア太平洋、ラテンアメリカ、中東・アフリカ |
公表された業界情報に基づく市場予測によると、バイオ医薬品の開発・製造の著しい拡大に加え、製品品質を確保するための厳格な安全性試験への需要の高まりを背景に、2031年まで堅調な成長が見込まれています。しかし、高度な試験装置の高コスト、専門知識の不足、および地域間の規制の相違が、市場のさらなる拡大を抑制する主要な要因として残ると予想されます。
「2025年の生物製剤安全性試験市場において、製品別ではアッセイ、キット、試薬セグメントが最大のシェアを占めました。」
製品別に見ると、生物製剤安全性試験市場は、アッセイ、キット・試薬、および機器に大別されます。2025年、アッセイ、キット、および試薬は、エンドトキシン、マイコプラズマ、無菌性、およびウイルス検出試験などの日常的な用途で広く使用されていることを背景に、生物製剤安全性試験市場において最大のシェアを占めました。その使いやすさ、信頼性、および自動化・ハイスループットシステムとの互換性により、これらの製品はあらゆる研究所において不可欠なものとなっています。さらに、その費用対効果の高さと、迅速かつ再現性のある結果を提供する能力が、世界中のバイオ医薬品企業、CRO、研究機関からの安定した需要を支えています。
「2025年、生物製剤安全性試験製品の用途別市場において、モノクローナル抗体および治療用タンパク質セグメントが最大のシェアを占めました。」
用途別に見ると、世界の生物製剤安全性試験製品市場は、ワクチン、モノクローナル抗体および治療用タンパク質、細胞・遺伝子治療製品、血液および血液製剤、その他の用途に分類されます。2025年、生物製剤安全性試験製品市場において、モノクローナル抗体および治療用タンパク質セグメントが最大のシェアを占めました。これは、慢性疾患や複雑な疾患の治療におけるこれらの製剤の広範な使用に牽引されたものです。これらの生物製剤のパイプラインの拡大、承認件数の増加、および大規模な商業生産には、厳格な安全性試験が求められます。さらに、厳格な規制要件や、製品の純度、効力、および一貫性を確保する必要性が、世界的に見て同セグメントの市場での地位をさらに強固なものにしています。
「2026年から2031年にかけて、生物製剤安全性試験市場において、アジア太平洋地域が最も高いCAGRで成長しています。」
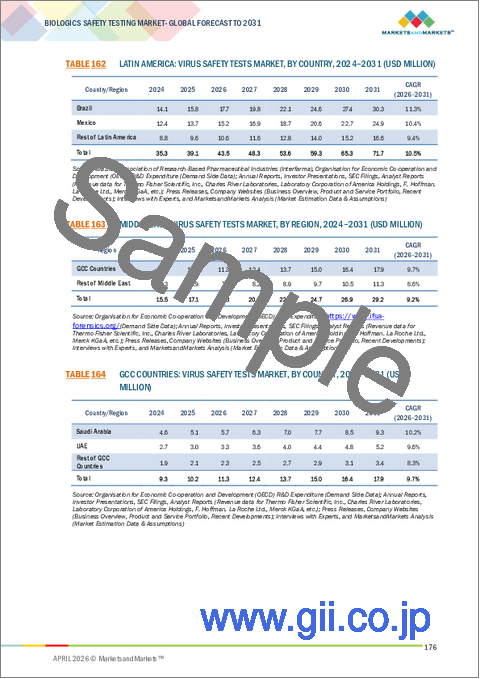
生物製剤安全性試験市場は、北米、欧州、アジア太平洋、ラテンアメリカ、中東・アフリカに区分されます。予測期間中、アジア太平洋地域は、バイオ医薬品製造の拡大、バイオ医薬品およびバイオシミラーの採用増加、ならびに臨床試験活動の活発化に支えられ、最も高いCAGRで成長すると推定されています。さらに、規制枠組みの改善も成長を後押ししており、サムスン・バイオロジクスやウーシー・アプテックといった主要な地域および世界の企業の存在が、バイオ医薬品の開発および安全性試験能力を積極的に強化しています。
当レポートで取り上げた企業プロファイル一覧
- Thermo Fisher Scientific Inc.
- Merck KGaA
- Lonza
- FUJIFILM Corporation
- Sartorius AG
- F. Hoffmann- La Roche Ltd.
- Charles River Laboratories
- bioMerieux
- WuXi AppTec
- SGS Societe Generale de Surveillance SA
- Sotera Health
- Samsung Biologics
- GenScript
- Agilent Technologies, Inc.
- Syngene International Limited
- Eurofins Scientific
- Laboratory Corporation of America Holdings
- Bio-Rad Laboratories, Inc.
- QIAGEN
調査範囲
本調査レポートでは、生物製剤安全性試験市場を、提供内容、試験の種類、用途(製品およびサービスの用途)、エンドユーザー(製品およびサービスのエンドユーザー)、および地域ごとに分類しています。調査範囲には、生物製剤安全性試験市場の成長に影響を与える主要な要因(促進要因、課題、機会、および制約)に関する詳細情報が含まれています。主要な業界企業について詳細な分析を行い、事業概要、製品ポートフォリオ、製品およびサービスの承認・発売、提携、パートナーシップ、事業拡大、契約、ならびに生物製剤安全性試験市場に関連する最近の動向といった主要戦略に関する洞察を提供しています。当レポートでは、生物製剤安全性試験市場のエコシステムにおける主要企業および新興スタートアップの競合考察を網羅しています。
当レポートを購入する主なメリット
当レポートは、生物製剤安全性試験市場全体およびそのサブセグメントの売上高に関する最も正確な推計値を提供することで、市場リーダーや新規参入企業の支援となります。また、利害関係者が競合情勢をより深く理解し、ビジネスをより効果的に位置付け、適切な市場参入戦略を策定するための洞察を得るのに役立ちます。当レポートは、利害関係者が市場の動向を把握できるようにし、主要な市場促進要因、抑制要因、機会、課題に関する情報を提供します。
当レポートでは、以下のポイントに関する洞察を提供します:
- 主要な促進要因(増加するバイオ医薬品およびバイオシミラーのパイプライン、厳格かつ進化する規制要件、細胞・遺伝子治療やmRNA製品などの先進的治療法の成長、CDMOの拡大および試験の外部委託への構造的シフト)、制約要因(先進的な試験装置の高コストおよび専門知識の不足、地域間の規制の相違)、機会(次世代治療薬への注目の高まり、動物を使用しない試験手法への移行)、および課題(アッセイの標準化におけるギャップ)など、生物製剤安全性試験市場の成長に影響を与える要因について分析しています
- 製品開発/イノベーション:生物製剤安全性試験市場における新発売製品に関する詳細な分析
- 市場開発:収益性の高い市場に関する包括的な情報-当レポートでは、様々な地域における生物製剤安全性試験市場を分析しています
- 市場の多様化:生物製剤安全性試験市場における新製品、未開拓地域、最近の動向、および投資に関する網羅的な情報
- 競合分析:Thermo Fisher Scientific Inc.(米国)、Merck KGaA(ドイツ)、Lonza(スイス)、FUJIFILM Corporation(日本)、Sartorius AG(ドイツ)、F. Hoffmann-La Roche Ltd.(スイス)、Charles River Laboratories(米国)などの主要企業の市場シェア、成長戦略、製品ラインナップに関する詳細な評価
よくあるご質問
目次
第1章 イントロダクション
第2章 エグゼクティブサマリー
第3章 重要考察
第4章 市場概要
- 市場力学
- 促進要因
- 抑制要因
- 機会
- 課題
- アンメットニーズと未開拓分野
- 相互接続された市場と異業種間の機会
- ティア1/2/3企業による戦略的な動き
第5章 業界動向
- ポーターの5つの競争要因分析
- マクロ経済見通し
- バリューチェーン分析
- エコシステム分析
- 価格分析
- 主要な会議およびイベント
- 顧客企業の事業に影響を与える動向/変化
- 投資・資金調達活動
- 米国関税が生物製剤安全性試験市場に与える影響
第6章 技術進歩、AIによる影響、特許、イノベーション、そして将来の応用
- 主要技術
- 隣接技術
- 補完的技術
- 技術/製品ロードマップ
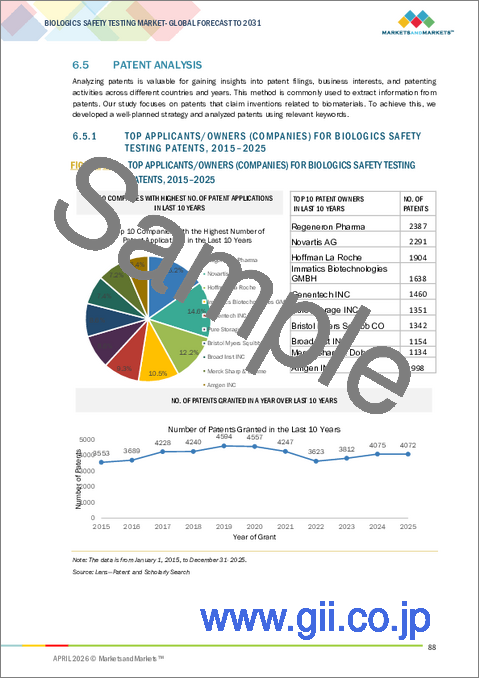
- 特許分析
- 将来の応用
- AI/生成AIが生物製剤の安全性試験市場に与える影響
第7章 規制状況と持続可能性への取り組み
- 地域規制および遵守事項
- 規制機関、政府機関、その他の組織
- 規制枠組み
- 業界標準
- 持続可能性への影響と規制政策イニシアチブ
- 認証、ラベル表示、および環境基準
第8章 顧客情勢と購買行動
- 意思決定プロセス
- 購入者の利害関係者と購入評価基準
- 導入における障壁と内部課題
- 様々な最終用途産業におけるアンメットニーズ
- 市場収益性
第9章 生物製剤安全性試験市場(オファリング別)
- サービス
- 製品
第10章 生物製剤安全性試験市場(試験タイプ別)
- ウイルス安全性検査
- 滅菌試験
- エンドトキシン検査
- マイコプラズマ検査
- 微生物汚染度検査
- 残留HCPおよびDNA検出検査
- その他
第11章 生物製剤安全性試験製品市場(用途別)
- モノクローナル抗体および治療用タンパク質
- ワクチン
- 細胞・遺伝子治療製品
- 血液および血液製剤
- その他
第12章 生物製剤安全性試験サービス市場(用途別)
- モノクローナル抗体および治療用タンパク質の安全性試験
- ワクチンの安全性試験
- 細胞・遺伝子治療の安全性試験
- 血液および血液製剤の安全性検査
- その他
第13章 生物製剤安全性試験製品市場(エンドユーザー別)
- 製薬・バイオテクノロジー企業
- CRO、CDMO
- 学術・研究機関
- その他
第14章 生物製剤安全性試験サービス市場(エンドユーザー別)
- 製薬・バイオテクノロジー企業
- 学術・研究機関
- その他
第15章 生物製剤安全性試験市場(地域別)
- 北米
- 米国
- カナダ
- 欧州
- ドイツ
- 英国
- フランス
- イタリア
- スペイン
- その他
- アジア太平洋
- 中国
- 日本
- インド
- 韓国
- オーストラリア
- その他
- ラテンアメリカ
- ブラジル
- メキシコ
- その他
- 中東
- GCC諸国
- その他
- アフリカ
- 普及促進のための意識向上と協働的な取り組み
第16章 競合情勢
- 主要参入企業の戦略/強み
- 収益分析
- 市場シェア分析
- 企業評価マトリックス:主要企業、2025年
- 企業評価マトリックス:スタートアップ/中小企業、2025年
- 企業評価と財務指標
- ブランド/製品比較分析
- 競合シナリオ
第17章 企業プロファイル
- 主要参入企業
- THERMO FISHER SCIENTIFIC INC.
- CHARLES RIVER LABORATORIES
- LABORATORY CORPORATION OF AMERICA HOLDINGS
- F. HOFFMANN-LA ROCHE LTD.
- MERCK KGAA
- SARTORIUS AG
- LONZA
- FUJIFILM CORPORATION
- BIOMERIEUX
- MARAVAI LIFESCIENCES
- WUXI APPTEC
- SGS SOCIETE GENERALE DE SURVEILLANCE SA
- SOTERA HEALTH
- SAMSUNG BIOLOGICS
- GENSCRIPT
- AGILENT TECHNOLOGIES, INC.
- SYNGENE INTERNATIONAL LIMITED
- EUROFINS SCIENTIFIC
- BIO-RAD LABORATORIES, INC.
- QIAGEN
- その他の企業
- PROMEGA CORPORATION
- CATALENT, INC.
- ASSOCIATES OF CAPE COD, INC.
- CLEAN BIOLOGICS
- PATHOQUEST
- PACIFIC BIOLABS
- ARL BIO PHARMA, INC.
- FRONTAGE LABS
- CREATIVE BIOGENE
- ADVAXIA BIOLOGICS