|
|
市場調査レポート
商品コード
2005192
間葉系幹細胞/治療用シグナル伝達細胞(MSCs):進展と応用(2026年)Mesenchymal Stem Cells / Medicinal Signaling Cells (MSCs) - Advances & Applications, 2026 |
||||||
|
|||||||
| 間葉系幹細胞/治療用シグナル伝達細胞(MSCs):進展と応用(2026年) |
|
出版日: 2026年01月30日
発行: BioInformant
ページ情報: 英文 381 Pages
納期: 即納可能
|
概要
エグゼクティブサマリー
MSCは、その汎用性と多様な応用を反映して、間葉系幹細胞、治療用シグナル伝達細胞、あるいは間葉系支持細胞などと呼ばれてきた多能性細胞です。MSCは、骨芽細胞、軟骨細胞、筋細胞、脂肪細胞など、様々な細胞タイプに分化することができます。組織修復を促進する因子を分泌し、抗炎症作用や抗線維化作用によって微小環境を調節するという独自の能力により、MSCは再生医療において不可欠な存在となっています。さらに、その免疫回避特性により、MSCは同種移植に特に適しています。
MSCは、再生医療、コスメシューティカル、培養肉生産など、数多くの産業において不可欠な原料として機能しています。主な応用分野には以下が含まれます:
- 筋骨格系疾患、脊髄損傷、および心血管疾患に対する細胞療法。
- 皮膚、骨、血管、肝臓などの人工組織および臓器。
- 化粧品やスキンケア製品に利用される、エクソソームや成長因子などの細胞由来製品。
- 筋肉の発達におけるMSCの役割や、筋肉細胞や脂肪細胞へ分化できる能力を活用した培養肉の生産。
世界的に、12のMSCを用いた治療法が様々な適応症で承認されており、その大半は韓国、日本、EUに集中しています。
具体的には、韓国では5つの製品が承認されています。Anterogenの「Queencell」、Pharmicellの「Cellgram AMI」、Anterogenの「Cupistem」、Medipostの「Cartistem」、およびCorestemの「NeuroNataR」です。日本では、JCR Pharmaceuticalsの「Temcell HS」とNipro Corporationの「Stemirac」の2つの製品が承認されています。欧州のEMAは、Chiesi Farmaceuticiの「Holoclar」と、TiGenix/Takedaの「Alofisel」の2製品を承認しました。インドは、Stempeuticsの「Stempeucel」を1製品承認しました。イランは、Cell Tech Pharmedが開発した「MesestroCell」を1製品承認しました。最後に、オーストラリアは、Mesoblastの「Remestemcel-L」を1製品承認しました。
こうした進展にもかかわらず、MSC(間葉系幹細胞)を基盤とした治療薬で米国FDAの承認を受けたものはまだありませんが、FDAはメソブラスト社の「Remestemcel-L」について積極的に審査を進めています。
コスメシューティカル市場でも、MSC由来製品、特にエクソソームが、その抗加齢作用や再生能力を活用するために急速に採用されており、L'OrealやJohnson & Johnsonといった企業がこの分野に多額の投資を行っています。同様に、培養肉企業も、味や食感を向上させるために、筋肉細胞や脂肪細胞の生産にMSCを活用しています。Upside FoodsやGood Meatによる培養鶏肉などの画期的な承認は、この業界のさらなる成長への道を開きました。
MSCを用いた遺伝子編集技術も拡大しており、抗腫瘍遺伝子や治療因子の過剰発現が可能になっています。また、研究者たちは3Dプリンティングや人工臓器の製造におけるMSCの活用も模索しており、今後10年間で画期的な進展が期待されています。
重要な点として、Cynata Therapeuticsのような企業はiPS細胞由来のMSC生産技術を先駆けて開発しており、これにより大規模な治療薬開発が可能となっています。現在、Cynata Therapeutics、Eterna Therapeutics、Implant Therapeutics、Bone Therapeutics、Brooklyn ImmunoTherapeutics、Fujifilm CDI、Citius Pharmaceuticals、Kiji Therapeuticsを含む、少なくとも8社がiPS細胞由来MSC(iMSC)治療薬の開発に携わっています。
また、ClinicalTrials.govには、MSCを対象とした1,670件以上の臨床試験が登録されています。これらの臨床研究の約75%(4分の3)は、再生医療(RM)製品の開発にMSCを使用しています。約14%の研究では、疾患モデル化にMSCが使用されています。残りの11%の研究では、創薬や細胞毒性試験の用途にMSCが使用されています。
これらの試験における課題には、増殖過程におけるMSCの表現型および機能性の維持が含まれます。しかし、継続的な進歩により将来性は有望視されており、2040年までに世界で少なくとも50のMSCベースの製品が承認され、年間平均3~4件の新規承認が見込まれています。
MSC調査用製品の主要企業
近年、MSCを用いた調査用の製品の需要が急増しており、主要サプライヤーは製品ラインナップを拡大しています。RoosterBioのような企業は、サプライチェーンの産業化、標準化された細胞バンク製品の形態、および目的に適合したcGMP準拠の細胞および培地システムを通じて、高品質なMSCへのアクセスを拡大しています。
その他の主要なMSC研究用製品サプライヤーには、PromoCell、Lonza、Thermo Fisher Scientific、STEMCELL Technologies、Miltenyi Biotec、Bio-Techne(R&D Systems)、ScienCell研究所、およびATCCなどが挙げられます。
課題と機会
MSCの商業化には、スケーラビリティや規制当局の承認といった障壁が存在する一方で、機会も数多く存在します。MSCベースの製品市場は、研究、治療、化粧品、食品産業の各分野において著しい成長が見込まれています。
この急速に変化する状況において、競合他社を徹底的に理解することは不可欠です。
本世界の戦略レポートでは、MSCに関する臨床試験、科学論文、特許、資金調達事例、および提携の動向を提示しています。また、MSCベースの治療薬のパイプラインを紹介し、市場の機会と脅威を特定するとともに、今後の方向性や新たな応用分野を探求しています。さらに、125社の主要競合企業が提供する革新的なMSC製品、サービス、技術についても明らかにしています。最後に、地域および事業セグメント別に分類した世界MSC市場の詳細な市場規模データと、2031年までの将来予測を提示しています。
目次
第1章 レポートの概要
- レポートの内容
- 対象層
- 本レポートの情報源
- レポートの目的
- 調査の最近の進歩
- 世界のMSC市場のサマリーを提供する
- 商業化の機会へのアクセス
- 主要な市場参入企業を特定し、競合環境を評価する
- 既存および新たな動向を特定する
- MSC市場における重要な機会と脅威を特定する
- エグゼクティブサマリー
- イントロダクション
第2章 間葉系幹細胞(MSC):概要
- ヒト間葉系幹細胞(hMSC)の安定化技術
- 間葉系幹細胞が再生医療に与える影響
- MSC命名法のタイムライン
- MSCの供給源
- 骨髄由来間葉系幹細胞(BM-MSC)
- 脂肪由来間葉系幹細胞(AD-MSC)
- 臍帯由来間葉系幹細胞(UC-MSC)
- iPSC由来間葉系幹細胞(iMSC)
- 間葉系幹細胞における細胞表面マーカー
- 間葉系幹細胞の体外分化能
- 間葉系幹細胞から分泌される可溶性因子
- 間葉系幹細胞に存在する幹細胞遺伝子
- MSCの種類とその生物医学的応用
- MSCの特性にとって重要な遺伝子
第3章 MSCを用いた臨床試験の現状
- 地域別のMSCを用いた臨床研究
- 現在の臨床試験で使用されているMSCの供給源
- 自家および同種MSCの臨床試験におけるシェア
- 疾患適応症別のMSCベースの臨床試験
- 研究段階別のMSCベースの臨床試験
- MSCを用いた臨床試験を選択する
- 筋骨格系疾患に対するMSCを用いた臨床試験
- 神経疾患に対するMSCを用いた臨床試験
- MSC由来エクソソームを用いた臨床試験
- 臨床試験におけるプライミング処理済みMSC
- 足場ベースのMSCを用いた臨床試験
第4章 間葉系幹細胞(MSCS):特許動向
- 管轄区域別MSC特許公開情報
- MSC特許出願人
- MSC特許発明者
- MSC特許権者
- MSC特許出願の法的地位
- MSC由来エクソソームに関する特許
- iPSC由来MSC(iMSC)に関する特許
- 治療タイプ別のMSC特許
第5章 MSCSに関する発表済みの科学論文
- PubMed.govに掲載された細胞療法におけるMSCに関する論文
- PubMed.govに掲載されたMSCベースの免疫療法に関する論文
- PubMed.govに掲載された遺伝子治療におけるMSCに関する論文
- PubMed.govに掲載された組織工学におけるMSCに関する論文
- PubMed.govに掲載された美容医療におけるMSCに関する論文
- 主要疾患におけるMSCの応用に関する発表論文数
- 改良型MSCに関する発表論文
- MSC由来エクソソームに関する発表論文
第6章 MSC製造プラットフォーム:概要
- 間葉系幹細胞の分離方法
- 細胞増殖:従来型培養からバイオリアクターへ
- 単層培養システム
- バイオリアクターを用いた細胞増殖
- 現在使用されているバイオリアクター
- MSC拡張システム:概要
- 技術別バッチあたりの細胞数
- 細胞増殖に用いられるマイクロキャリア
- MSCの下流工程
- 細胞の剥離と分離(収穫)
- 細胞の洗浄と濃縮
- 安全性および効力試験
- 間葉系幹細胞と線維芽細胞を区別するための表面マーカー
- 自家および同種MSC製造:比較
- 同種間葉系幹細胞の製造コスト
- 自家MSCの製造コスト
- ドナーのスクリーニングと検査にかかる費用
- リリース試験の費用
- MSCの大規模製造
- MSC製造プラットフォーム
- 細胞培養容器のスケールアップ
- 培養培地
- 間葉系幹細胞の凍結保存
第7章 細胞・遺伝子治療の受託製造
- 人員不足
- 自動化の必要性
- 容量制約
- より大きな可能性を秘めたCDMOプラットフォーム
- CMO/CDMO
- 医薬品製造受託機関(CMO)
- 医薬品開発・製造受託機関(CDMO)
- 製造施設の地理的分布
- アウトソーシングの継続的な増加
- 米国の主要なCDMO(医薬品受託製造開発機関)
- 欧州の主要細胞・遺伝子治療CDMO
- 欧州における受託製造業における英国の優位性
第8章 MSCの機能を向上させるためのバイオエンジニアリングソリューション
- 間葉系幹細胞の低分子プライミング
- MSCの粒子工学
- MSCの遺伝子工学
- 抗がん剤を生産するためのバイオエンジニアリングされたMSCの例
- 神経疾患に対する遺伝子操作されたMSC
- 心血管疾患治療のための遺伝子操作された間葉系幹細胞
- 肺損傷治療のための遺伝子操作された間葉系幹細胞
- 糖尿病治療のための遺伝子操作されたMSC
- MSC投与を改善するためのバイオエンジニアリングアプローチ
第9章 MSCSが対象とする主な疾患
- 自己免疫疾患に対するMSCを用いた研究
- 心血管疾患に対するMSCを用いた研究
- 神経変性疾患に対するMSCを用いた研究
- 骨・軟骨疾患に対するMSCを用いた研究
- GVHDにおけるMSCを用いた研究
- クローン病におけるMSCを用いた研究
- 1型糖尿病におけるMSCを用いた研究
- 全身性エリテマトーデス(SLE)におけるMSCを用いた研究
- パーキンソン病におけるMSCを用いた研究
- アルツハイマー病におけるMSCを用いた研究
- 腎不全におけるMSCを用いた研究
- 脊髄損傷におけるMSCを用いた研究
- 間葉系幹細胞を用いた創傷治癒に関する研究
第10章 MSC分野における最近の協力関係(2020年~2024年)
- BioSolution DesignsとRoosterBioの提携
- CytoMed Therapeutics, Ltd.とSengkang General Hospitalの提携
- REPROCELLとHistocellの提携
- FUJIFILM DiosynthとRoosterBioの提携
- RoosterBioとAGC Biologicsの提携
- RoosterBioとShiftBioの提携
- RoosterBioとUnivercells Technologiesの提携
- CynataとFujifilmの提携
- American CryoStem Corp.とBioTherapeutic Lab Corp.の提携
- RoosterBioとSartoriusの提携
- American CryoStemとCRADAの提携
- RoosterBioとSartorius Korea Biotechの提携
- CatalentとBrainStormの提携
- CiplaとStempeuticsの提携
- AethlonとUniversity of Pittsburghの提携
- RoosterBioとSenti Biosciencesの提携
第11章 世界市場におけるMSCベース製品
- 承認されたMSC療法
- クイーンセル
- セルグラムAMI
- クピステム
- カルティステム
- NeuroNataR
- ホロクラル
- 原基質/ ライオンシル(レメステムセル-L)
- テムセルHS
- ステムペウセル
- MesestroCell
- ステミラック
- ルイボシェン(アミメストロセル)
- 市販の生体材料担体ベースのMSCおよびMSC前駆細胞
- Osteocel
- AlloStem
- Grafix
- Cellentra VCBM
- Trinity ELITE
- Map3
- BIO4
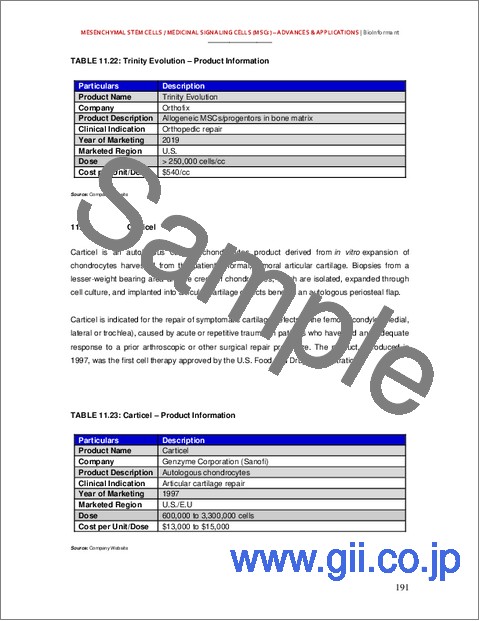
- Trinity Evolution
- Carticel
- Chondron
- DeNovo NT
- Ossron
- JACC
- MACI
- Ortho-ACI
- Ossgrow
- Cartigrow
- MSC/MSC由来エクソソームを含む局所用化粧品
第12章 市場分析
- MSC療法の市場規模
- 間葉系幹細胞(MSC)の世界の需要
第13章 企業プロファイル
- Advancells
- Aegle Therapeutics
- AGC Biologics
- AlloSource, Inc.
- Ambulero
- American CryoStem Corporation
- American Type Culture Collection (ATCC)
- Amniotics
- Andelyn Biosciences
- Anemocyte Srl
- Anterogen, Co., Ltd.
- Avid Bioservices, Inc.
- Bacthera
- Baylx, Inc.
- BioCardia
- BioCentriq
- BioEden, Inc.
- Bioinova s.r.o
- BioRestorative Therapies
- Bioscience Institute S.p.A
- Blue Horizon International, LLC
- Boehringer Ingelheim BioXellence
- Bonus Biogroup, Ltd.
- BrainStorm Cell Therapeutics, Inc.
- Catalent
- CCRM
- Cell2Cure ApS
- Cell Care Therapeutics
- Cellcolabs
- CELLeBRAIN
- Cellipont Bioservices
- Celprogen, Inc.
- CellProthera
- CellResearch Corporation, Pte, Ltd.
- Cell Surgical Network (CSN)
- Celltex Therapeutics Corporation
- CellTherapies
- Cellular Biomedicine Group
- Charles River Laboratories
- CHIESI Farmaceutici S.p.A
- Citius Pharmaceuticals, Inc.
- CorestemChemon, Inc.
- Creative Bioarray
- Creative Medical Technology Holdings, Inc.
- Curia Global, Inc
- Cynata Therapeutics, Ltd
- Cytovance Biologics
- Defined Bioscience, Inc.
- Direct Biologics
- eQcell, Inc.
- Excellos
- Exosla Therapeutics
- EXOSOMEplus
- Exothera
- Fujifilm Diosynth Biotechnologies
- Future Cell Japan, Co., Ltd
- Genezen
- GenScript Biotech Corporation
- Hope Biosciences, LLC
- Implant Therapeutics, Inc
- INCELL Corporation LLC
- InGeneron GmbH
- Invitrx Therapeutics
- Japan Tissue Engineering, Co., Ltd. (J-TEC)
- JCR Pharmaceuticals, Co., Ltd.
- Jointechlabs
- Kangstem Biotech, Co., Ltd
- Kimera Labs
- LifeCell
- Longeveron
- Lonza Group, Ltd
- Lorem Cytori USA, Inc.
- MEDPOST
- Mesoblast, Ltd.
- Millipore Sigma
- NecstGen
- NextCell
- NIPRO Corporation
- Novadip Biosciences
- Novus Biologicals, LLC
- NuVasive
- OCT Therapies & Research Pvt., Ltd
- OmniaBio, Inc.
- Orthocell, Ltd
- Orthofix Medical, Inc.
- Ossium Health
- Personal Cell Sciences Corporation
- Personalized Stem Cells, Inc.
- Pfizer CentreOne
- Pluri Biotech, Ltd.
- Porton Advanced
- Prometheus Life Technologies
- PromoCell GmbH
- PuREC, Co., Ltd.
- Regrow Biosciences
- Reliance Life Sciences, Pvt., Ltd.
- Remedy Cell, Ltd.
- Rentschler Biopharma
- REPROCELL USA, Inc
- Resilence
- RESTEM, LLC
- RHEACELL GmbH &Co., KG
- Richter-HELM
- RoosterBio, Inc.
- RTI Surgical
- RoslinCT
- Samsung Biologics
- San Bio, Co., Ltd.
- Smith & Nephew, Inc.
- StemBioSys, Inc.
- STEMCELL Technologies, Inc
- Stemedica Cell Technologies, Inc.
- Stemmatters
- StemMedical
- Stempeutics Research Pvt., Ltd
- StromaBio AB
- TaiwanBio Therapeutics, Co., Ltd.
- Takeda Pharmaceutical, Co., Ltd
- Tempo Bioscience
- ThermoFisher Scientific
- Vericel Corporation
- Wuxi App Tec
- Xintela AB