
|
市場調査レポート
商品コード
2035078
契約研究機関:市場シェア分析、業界動向と統計、成長予測(2026年~2031年)Contract Research Organization - Market Share Analysis, Industry Trends & Statistics, Growth Forecasts (2026 - 2031) |
||||||
カスタマイズ可能
適宜更新あり
|
|||||||
| 契約研究機関:市場シェア分析、業界動向と統計、成長予測(2026年~2031年) |
|
出版日: 2026年01月06日
発行: Mordor Intelligence
ページ情報: 英文 115 Pages
納期: 2~3営業日
|
概要
契約研究機関(CRO)市場の規模は、2026年に929億8,000万米ドルと推計されており、予測期間(2026年~2031年)においてCAGR8.27%で推移し、2031年までに1,383億4,000万米ドルに達すると見込まれています。
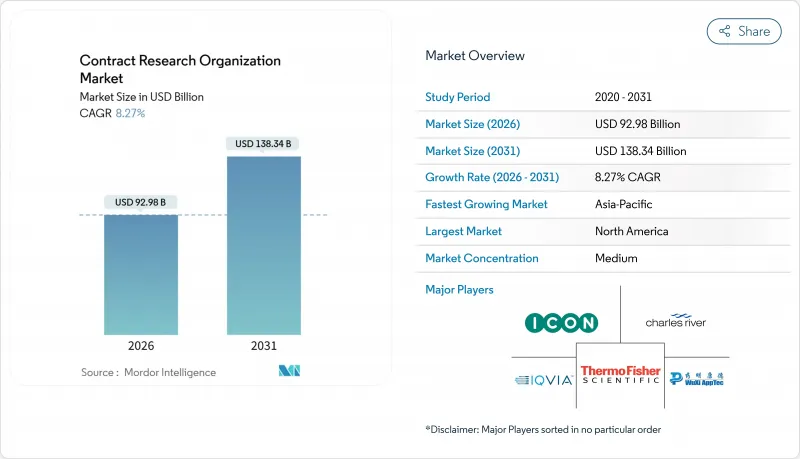
収益の拡大は、開発サイクルの短縮、世界の患者へのアクセス確保、そしてますます複雑化する規制プロセスへの準拠を求めるスポンサーのニーズの高まりによって牽引されています。生物製剤や細胞・遺伝子治療への投資により、臨床試験のポートフォリオは、社内で実施できるスポンサーがほとんどいないような高度に複雑なプロトコルへと移行しています。規制当局は引き続き迅速審査指定を付与しており、これにより審査期間が短縮され、重要な機能の外部委託がさらに促進されています。初期段階のバイオテクノロジー企業へのベンチャーキャピタルの流入は、ヒト初臨床試験に関する専門知識への需要を支えており、一方でテクノロジーを活用した治験施設選定ツールは、立ち上げまでの期間を短縮し、スクリーニングの失敗率を低下させています。
世界のCRO市場の動向とインサイト
バイオ医薬品および先進的治療法の開発件数の増加
バイオ医薬品や細胞・遺伝子治療のパイプラインには、ウイルスベクターの製造、体外での細胞操作、および長期的な患者モニタリングが必要ですが、これらを社内で保有しているスポンサーはほとんどありません。FDAの「再生医療先進療法(Regenerative Medicine Advanced Therapy)」指定は製品の適格性審査を迅速化し、適応型デザインや分散型サンプル物流を管理できるCROにメリットをもたらしています。新たなCMCガイドラインによりIND申請の不確実性が軽減され、低分子医薬品ポートフォリオからバイオ医薬品への資本再配分が進んでいます。バイオシミラーが既存製品の収益を圧迫する中、スポンサーは、長期にわたる遺伝子編集臨床試験に必要な高度に専門化されたインフラを提供するために、CROパートナーに依存しています。
新興市場における患者プールと治験施設の拡大
中国の多地域臨床試験枠組みは現在、海外データを承認しており、多国籍プログラムにおける治験施設の立ち上げを加速させています。インドの中央医薬品標準管理機構(CDSCO)は審査サイクルを短縮し、治療経験のない患者コホートを求める腫瘍学および代謝疾患のスポンサーを惹きつけています。ブラジルのANVISAはICH E6(R2)に準拠し、行政上の摩擦を軽減するとともに、ラテンアメリカにおける被験者登録を促進しています。これらの地域における人口構成の広さは、迅速な被験者登録を可能にし、民族的に多様なデータセットを通じて規制当局への申請を強化します。
品質監査とコンプライアンス違反に対する罰則の強化
FDAは、適正臨床試験実施基準(GCP)を徹底するため、治験責任医師、IRB、および治験依頼者を検査しており、これによりCROはモニタリング、電子監査証跡、および第三者検証に、より大きな予算を割り当てるよう迫られています。EMAの臨床試験情報システムは透明性を高め、それによって評判のリスクを高めています。コンプライアンスコストが上昇する中、小規模なプロバイダーは利益率の圧迫や統合のリスクに直面しています。
セグメント分析
CRO市場で最も急成長しているセグメントである初期段階開発サービスは、2031年まで年率10.72%で拡大すると予測されています。金額ベースでは、バイオテクノロジー企業のスポンサーが迅速な概念実証(PoC)プログラムを優先するにつれ、このセグメントがCRO市場規模に占める割合は増加していく見込みです。臨床研究サービスは依然として支配的な地位を維持し、2025年には売上高シェアの61.45%を占める見込みですが、調達審査の厳格化により価格の上昇は抑制されています。第I相試験部門は、専用の施設、経験豊富なメディカルモニター、および学術機関への即時アクセスを有しており、これらがヒト初試験のリスクを軽減するため、プレミアムな料金設定が可能となっています。第II相および第III相の業務は、電子データ収集(EDC)の普及により差別化が薄れ、コモディティ化が進んでいます。一方、検査サービスはプレシジョン・メディシンへの需要に応じ着実に成長しており、コンサルティングサービスは複雑な規制戦略においてニッチな需要を維持しています。
スポンサーはバイオマーカー選別コホートの導入を拡大しており、これにより被験者数は減少するもの、解析の複雑さは増しています。フェーズIVのサーベイランスは、規制当局が承認後の安全性データの提出を求めることから緩やかに拡大していますが、多くの大手スポンサーは実世界データに対する管理権を維持するため、これらの研究を自社内で行うようになっています。差別化の焦点は、技術プラットフォーム、適応型デザインに関する専門知識、および分散型試験要素のシームレスな統合へと移行しています。この二極化により、初期段階の活動ではプレミアム価格を維持できる一方、成熟したサービスは運営規模で競争することになります。
オンコロジーは、免疫療法、標的低分子薬、細胞療法を含む1,000件以上の進行中の臨床資産の恩恵を受け、2025年には21.43%と、治療領域の中で最も大きな収益を生み出しました。一方、感染症領域は、パンデミック対策への投資やmRNAワクチンプラットフォームを背景に、2031年までのCAGR10.81%と最も急速な拡大を示しています。中枢神経系および免疫学の各領域も、主観的な評価の必要性を低減するデジタルバイオマーカーの普及に支えられ、それぞれ多額の投資を集めています。心血管および呼吸器系の各カテゴリーは、ジェネリック医薬品による市場侵食により研究開発資金が希少疾患へとシフトしているため、後れを取っています。
抗菌薬開発に対する政府のインセンティブと、刷新されたワクチンパイプラインが、感染症分野の勢いを支えています。腫瘍学分野の減速は、衰退ではなく成熟の表れです。すでに市販化されたチェックポイント阻害剤は、後期臨床試験から市販後の取り組みへと活動が移行しています。中枢神経系(CNS)のプログラムは依然として高いスクリーニング失敗率と長期にわたる追跡期間に直面しており、神経学の専門家や強固な治験責任医師ネットワークを擁するCROとの連携が不可欠となっています。希少疾患の特定は依然としてボトルネックとなっており、独自の患者登録データベースを持つCROには競争上の優位性が生まれています。
本「医薬品開発受託機関(CRO)市場レポート」は、サービスタイプ(初期段階開発など)、治療領域(オンコロジー、感染症など)、エンドユーザー(製薬・バイオ医薬品、医療機器、その他)、提供モデル(フルサービス、FSP、ハイブリッド)、および地域(北米、欧州、アジア太平洋、中東・アフリカ、南米)ごとに分類されています。市場予測は金額(米ドル)で提示されています。
地域別分析
北米は2025年に売上高の38.92%を占め、米国における35万カ所の研究インフラとFDAの世界の規制上の影響力がその基盤となっています。スポンサーがコスト抑制や多様な患者層へのアクセスを目的として多角化を進める中、成長率はCRO市場平均を下回っています。カナダとメキシコは迅速な倫理審査承認を通じて心血管疾患および糖尿病のコホートを提供しており、一方、米国の学術研究機関は複雑な腫瘍学および遺伝子治療のプロトコルを維持しています。
アジア太平洋地域は、規制の近代化と治療未経験の膨大な患者層に牽引され、2031年までにCAGR11.26%を記録する見込みであり、これはCRO市場において最も急速な地域成長軌道となります。中国では、IND審査の効率化や多国籍臨床試験(MRCT)における外国データの承認により、世界のプログラムへの参加が促進されています。インドでは審査サイクルの短縮により腫瘍学分野の被験者登録が加速しており、日本ではICH準拠により多国籍申請が容易になっています。オーストラリアは、研究開発税額控除や迅速な倫理審査を活用し、ヒト初試験の誘致に力を入れています。韓国は細胞療法のインフラに多額の投資を行っており、先進的治療法の臨床試験が増加しています。
欧州は、EMA(欧州医薬品庁)の臨床試験情報システムを通じた承認の調和により、成熟した第III相試験の実施能力を維持しています。ドイツ、英国、フランスは依然として中核的な拠点ですが、ブレグジットにより、現在は英国向けの並行プロトコルが必要となっています。スペインとイタリアは相対的なコスト面での優位性を持ち、呼吸器系および循環器系の臨床試験を徐々に獲得しています。中東およびアフリカは規模は小さいもの、湾岸諸国が研究の多角化に投資していることから、希少疾患やワクチンの臨床試験を受け入れています。一方、南米では、ブラジルとアルゼンチンを中心に、規制の調和が進む中で感染症の調査の分野で存在感を高めています。
その他の特典:
- エクセル形式の市場予測(ME)シート
- 3ヶ月間のアナリストサポート
よくあるご質問
目次
第1章 イントロダクション
- 調査の前提条件と市場の定義
- 調査範囲
第2章 調査手法
第3章 エグゼクティブサマリー
第4章 市場情勢
- 市場概要
- 市場促進要因
- バイオ医薬品および先進的治療法の開発件数の増加
- 新興市場における患者層および治験施設の拡大
- 希少疾病用医薬品およびファストトラック医薬品に対する規制審査の迅速化
- 初期段階のバイオテクノロジー企業に対するベンチャーキャピタル資金調達の拡大
- 分散型/ハイブリッド型臨床試験アーキテクチャの採用
- 実世界データとデジタルバイオマーカーの統合による開発期間の短縮
- 市場抑制要因
- 品質監査の強化とコンプライアンス違反に対する罰則の厳格化
- 最先端のラボオートメーションに向けた多額の設備投資
- 国境を越えた臨床試験に影響を与える地政学的リスクの高まり
- GMP基準を満たすウイルスベクター製造能力の不足
- 規制の見通し
- ポーターのファイブフォース分析
- 新規参入業者の脅威
- 供給企業の交渉力
- 買い手の交渉力
- 代替品の脅威
- 業界間の競争
第5章 市場規模と成長予測
- サービスタイプ別
- 初期段階の開発サービス
- 臨床調査サービス
- 第I相
- 第II相
- 第III相
- 第IV相
- 検査サービス
- コンサルティングサービス
- 治癒領域別
- オンコロジー
- 感染症
- 中枢神経系(CNS)疾患
- 免疫系疾患
- 心血管疾患
- 呼吸器疾患
- 糖尿病
- その他の治療領域
- エンドユーザー別
- 製薬・バイオ医薬品企業
- 医療機器メーカー
- その他のエンドユーザー(学術機関/政府機関)
- 提供モデル別
- フルサービス/統合型CRO
- 機能別サービスプロバイダー(FSP)
- ハイブリッド/モジュラーモデル
- 地域
- 北米
- 米国
- カナダ
- メキシコ
- 欧州
- ドイツ
- 英国
- フランス
- イタリア
- スペイン
- その他欧州地域
- アジア太平洋地域
- 中国
- 日本
- インド
- オーストラリア
- 韓国
- その他アジア太平洋地域
- 中東・アフリカ
- GCC
- 南アフリカ
- その他中東・アフリカ地域
- 南米
- ブラジル
- アルゼンチン
- その他南米
- 北米
第6章 競合情勢
- 市場集中度
- 市場シェア分析
- 企業プロファイル
- BioAgile Therapeutics Private Limited
- Charles River Laboratories
- CRITERIUM, INC.
- Evotec SE
- Eurofins Scientific
- Fortrea
- ICON Plc
- IQVIA Holdings Inc.
- Inotiv
- Medpace, Inc.
- Parexel International(MA)Corporation
- Pharmaron
- PSI
- SGS S.A.
- Syneos Health
- Syngene International Limited
- Thermo Fisher Scientific Inc.(PPD Inc.)
- Tigermed
- Worldwide Clinical Trials
- WuXi AppTec(WuXi Clinical)

