
|
市場調査レポート
商品コード
1911814
ポリピル製品:市場シェア分析、業界動向と統計、成長予測(2026年~2031年)Polypill Products - Market Share Analysis, Industry Trends & Statistics, Growth Forecasts (2026 - 2031) |
||||||
カスタマイズ可能
適宜更新あり
|
|||||||
| ポリピル製品:市場シェア分析、業界動向と統計、成長予測(2026年~2031年) |
|
出版日: 2026年01月12日
発行: Mordor Intelligence
ページ情報: 英文 120 Pages
納期: 2~3営業日
|
概要
ポリピル製品市場は、2025年の334億6,000万米ドルから2026年には341億8,000万米ドルへ成長し、2026年から2031年にかけてCAGR2.15%で推移し、2031年までに380億2,000万米ドルに達すると予測されております。
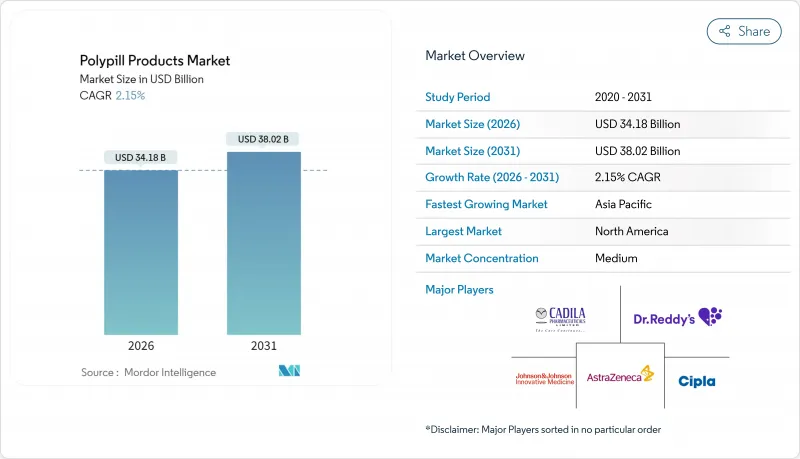
臨床的エビデンスの蓄積、世界保健機関(WHO)の必須医薬品リストへの掲載、規制面での支援的マイルストーンにより、固定用量配合剤は実験的コンセプトから主流の予防心臓病学ツールへと変貌を遂げました。3剤配合ポリピルが商業的な主導権を維持する一方、米国で初めて高血圧初期治療用3剤配合剤が承認されたことで、固定用量療法に対する医師の信頼が拡大しています。地理的な勢いはアジア太平洋地域へ移行しつつあり、心血管疾患の有病率上昇とインフラ投資が同地域で最も強い成長見通しを支えています。競合の激しさは、多国籍の革新企業とコスト優位性を持つ地域メーカーが競合する中、依然として中程度です。しかしながら、最近の承認とパイプラインへの投資は、特に超低用量4剤配合剤やデジタルヘルス対応製品において、製品発売頻度の加速を示唆しています。
世界の・ポリピル製品市場の動向と洞察
心血管疾患(CVD)および高血圧の有病率上昇
米国では約1億2,790万人の成人(人口の48.6%)が少なくとも1つの心血管疾患を抱えており、治療対象となる患者層は着実に拡大しています。高血圧は世界で12億人以上に影響を及ぼしていますが、主要経済国における管理率は50%を下回っており、ポリピルが埋められる持続的な治療格差が存在することを浮き彫りにしています。高所得国における人口の高齢化と新興市場における都市型ライフスタイルへの移行が相まって、この需要の増加傾向を支えています。米国では非ヒスパニック系黒人コミュニティが心血管疾患の負担を不均衡に背負っており、簡素化された固定用量療法は公平性を重視した介入策となります。医療システムが予防戦略を強化する中、単一の錠剤によるシームレスな多機序制御は処方医の関心を集めており、ポリピル製品市場の成長を後押ししています。
臨床試験のエビデンス拡大と研究開発パイプライン
26件のランダム化比較試験のメタ分析により、ポリピル療法は標準治療と比較して死亡率を11%低減し、心血管イベントを29%減少させることが示されました。SECURE試験では二次予防において主要心血管イベントが24%減少、PolyPars研究では一次予防環境でリスクが50%低減したと報告されています。これに対し、大手製薬企業はパイプラインの拡充で対応しています。アストラゼネカは189の心血管プロジェクトを保有し、メルクは最近、ファースト・イン・クラスの経口リポタンパク質(a)阻害剤であるHRS-5346のライセンシングを取得しました。2025年にFDAがウィダプリクを高血圧治療の初期療法として承認したことで、ポリピルは最終手段から第一選択薬へと地位を変え、世界の規制審査の進行を加速させました。これらの画期的な進展が相まって、科学的・商業的信頼性を高め、ポリピル製品市場を前進させています。
安全性および有害事象の異質性に関する懸念
構成薬剤の複合的なリスクプロファイルにより、低血圧、腎機能への影響、代謝変化に対する警戒が高まり、日常的な薬物監視を複雑化させています。医師は患者が副作用を経験した際の個別用量調整に懸念を抱き、規制当局は集団規模の安全性エビデンスを要求するため、開発期間が長期化しています。市販後調査では、どの有効成分が有害事象を引き起こしたかを特定する必要があり、これは複雑な作業であり、処方医を躊躇させる要因となり、慎重な市場における短期的な普及を抑制する可能性があります。
セグメント分析
2025年には三剤配合製剤が売上高の42.70%を占め、包括的なリスク因子カバーに対する医師の確固たる信頼を示し、ウィダプリク承認後の第一選択治療の基盤となっています。四剤以上配合製剤は4.12%のCAGRを示し、各成分の投与量を減らすことで副作用を最小限に抑えつつ有効性を維持する革新を牽引しています。QUARTET USA試験では4剤配合・1/4用量戦略が検証され、顕著な血圧低下と80%の患者満足度を達成しました。これらのデータは、段階的増量から即時的多経路制御への移行を加速させ、先進医療モデルにおけるポリピル製品の市場規模を支えています。デュアルクラスおよびシングルクラス製剤は増量柔軟性でニッチな存在感を維持しますが、ガイドラインが多剤配合錠の広範な採用を推奨する中、シェアは漸減傾向にあります。
超低用量四剤配合錠は、耐容性のトレードオフを最小限に抑えつつリスク因子を最大限抑制する方向への転換を示しています。系統的レビューでは目標血圧達成率90%が確認され、軽度の有害事象プロファイルにより治療中止に至るケースは稀です。実臨床での認知度が高まるにつれ、支払機関は入院回避効果を認識し、四剤配合ポリピル製品の市場シェアは2031年まで漸増的な拡大が見込まれます。
スタチン+降圧剤配合剤は、数十年にわたる安全性データとWHOによるアトルバスタチン系配合剤の推奨を背景に、2025年には32.40%のシェアを占めました。固定配合剤であるアトルバスタチン+アムロジピン5/20mg錠は、自由配合剤と比較して複合エンドポイントを大幅に低減し、二次予防における役割を確固たるものにしています。抗血小板薬の組み込みによりリスク低減効果が向上し、CNICポリピルは二次予防用途で欧州医薬品庁(EMA)の承認を取得。三成分配合剤は現在3.79%のCAGRで拡大中です。特に低中所得国(LMIC)の入札における普及が進む中、三成分スタチン配合ポリピル製品の市場規模は戦略的な拡大が見込まれます。
新たな製剤としては、スタチンにPCSK9阻害剤やSGLT2阻害剤を併用し、残存する脂質代謝リスクや代謝リスクに対処するものが登場しています。韓国におけるテルミサルタン/ロスバスタチン/アムロジピン/エゼチミブの4剤配合剤「ヌボロゼット」の2025年承認は、持続性脂質異常症というアンメットニーズを対象とした多機序作用型錠剤に対する規制当局の開放性を示しています。こうした革新は治療選択肢を多様化し、早期参入企業の競争優位性を強化します。
地域別分析
北米は2025年の売上高の40.15%を占めました。これは高度な償還制度、臨床試験インフラ、および第一選択高血圧治療におけるWidaplikの推奨によるものです。米国には1億2,200万人の高血圧成人が存在しますが、50%未満の管理率は採用の大きな余地を示しています。カナダでは中央集権的な医薬品審査により州レベルの保険適用が加速し、メキシコのセグロ・ポピュラー改革は固定用量調剤を維持しています。地域研究開発拠点ではQUARTET USAなどの重要なデータセットが生み出され、併用療法の主流化をさらに推進しています。
アジア太平洋地域は、拡大する中産階級人口、生活様式の変化、プライマリケアの普及拡大により、6.62%という最速のCAGRを記録しています。インドの製薬企業(心臓疾患治療薬ポートフォリオが10%成長したCiplaが代表例)は、国内市場および輸出市場向けに価格競争力のある供給を推進しています。中国の2024年高血圧ガイドラインは併用療法の有用性を強調し、韓国のNUVOROZET承認は規制面での進展を反映しています。日本とオーストラリアは臨床研究パイプラインとデジタルヘルス統合を推進し、技術主導型心臓病学における地域的リーダーシップを強化しています。
欧州、中東・アフリカ、南米は、それぞれ異なる特性を持つ機会環境を形成しています。欧州では欧州医薬品庁(EMA)によるCNIC複合薬の承認が二次予防プロトコルの基盤となり、恩恵を受けております。ナイジェリアとケニアの調達パイプラインはWHOの必須医薬品リスト掲載により推進力を得ており、アルゼンチンの経済的実現可能性(月間治療費が0.2~2.8日分の賃金に相当)が示されております。市場参入戦略は、異なる規制・償還・インフラ条件に対応する柔軟性が求められますが、心血管疾患罹患率の上昇が3大陸全体での持続的な需要を支えております。
その他の特典:
- エクセル形式の市場予測(ME)シート
- アナリストによる3か月間のサポート
よくあるご質問
目次
第1章 イントロダクション
- 調査の前提条件と市場の定義
- 調査範囲
第2章 調査手法
第3章 エグゼクティブサマリー
第4章 市場情勢
- 市場概要
- 市場促進要因
- 心血管疾患(CVD)及び高血圧の有病率上昇
- 臨床試験エビデンスの拡大と研究開発パイプライン
- 服薬遵守性の向上と多剤併用療法の比較
- FDC療法の費用対効果実証
- WHO必須医薬品リスト掲載が低中所得国における調達を促進
- ポリピル向けデジタルヘルス定期購入モデル
- 市場抑制要因
- 安全性及び有害事象の異質性に関する懸念
- 複雑な複数機関による規制承認
- 高温多湿気候下における製剤安定性
- 償還コードの欠如と支払者の消極性
- 規制情勢
- テクノロジーの展望
- ポーターのファイブフォース分析
- 新規参入業者の脅威
- 買い手の交渉力
- 供給企業の交渉力
- 代替品の脅威
- 競争企業間の敵対関係
第5章 市場規模と成長予測(金額:米ドル)
- 製品タイプ別
- 単一成分ポリピル
- デュアルクラスポリピル
- トリプルクラスポリピル
- クワッドクラス以上のポリピル
- 成分別
- スタチン+降圧剤
- 降圧剤+抗血小板剤
- スタチン+降圧剤+抗血小板剤
- その他
- 用途別
- 心血管疾患予防
- 糖尿病関連心血管疾患リスク低減
- 脳卒中予防
- その他
- 流通チャネル別
- 病院薬局
- 小売薬局
- オンライン薬局
- 地域別
- 北米
- 米国
- カナダ
- メキシコ
- 欧州
- ドイツ
- 英国
- フランス
- イタリア
- スペイン
- その他欧州地域
- アジア太平洋地域
- 中国
- 日本
- インド
- オーストラリア
- 韓国
- その他アジア太平洋地域
- 中東・アフリカ
- GCC
- 南アフリカ
- その他中東・アフリカ
- 南米
- ブラジル
- アルゼンチン
- その他南米
- 北米
第6章 競合情勢
- 市場集中度
- 市場シェア分析
- 企業プロファイル
- AstraZeneca
- Cadila Pharmaceuticals
- Cipla, Inc.
- Dr. Reddy's Laboratories
- Ferrer Internacional
- George Medicines
- Janssen(Johnson & Johnson)
- Merck & Co.
- Pfizer
- Takeda Pharmaceutical
- Amra Remedies
- East-West Pharma
- Excella Life Sciences
- Torrent Pharma
- Lupin
- Sun Pharmaceutical
- Teva Pharmaceutical
- Glenmark Pharma
- Viatris
- Aurobindo Pharma

