|
|
市場調査レポート
商品コード
1319156
肝がん診断の世界市場-2023年~2030年Global Liver Cancer Diagnostics Market - 2023-2030 |
||||||
カスタマイズ可能
適宜更新あり
|
|||||||
| 肝がん診断の世界市場-2023年~2030年 |
|
出版日: 2023年07月31日
発行: DataM Intelligence
ページ情報: 英文 195 Pages
納期: 即日から翌営業日
|
- 全表示
- 概要
- 目次
市場概要
肝がん診断の世界市場は、2022年に86億米ドルに達し、2023-2030年の予測期間中にCAGR 6.6%で成長し、2030年には141億米ドルに達すると予測されています。肝臓がんは、肝臓に発生し、体の他の部位に転移する可能性のある悪性腫瘍です。世界的に最も一般的ながんの1つです。肝臓がんを効果的に治療するには、早期診断が鍵となります。
現在、肝臓がんの診断にはいくつかの方法が用いられています。コンピュータ断層撮影(CT)スキャンや磁気共鳴画像法(MRI)などの画像検査や、特定のタンパク質やホルモンの濃度を測定する血液検査などです。また、検査用の細胞を採取するために生検を行うこともあります。医師は、利用可能な様々な診断方法を理解していれば、肝臓がんを効果的に発見し、効率的な治療戦略を立てることができます。早期診断は患者の予後を改善するために非常に重要です。
さらに、肝がんの有病率の増加、新規肝がん検出検査に対する承認の増加、肝がん診断のための画像診断システムの進歩が、予測期間中に市場を牽引すると予想される要因です。
市場力学
肝細胞がんの早期発見における技術進歩が世界の肝がん診断市場の成長を牽引すると期待される
2022年8月4日、UCLA Jonsson Comprehensive Cancer Centreの研究者が主導し、50人以上の研究者が参加した新しい研究によると、開発中の新技術は、原発性肝がんの80%から85%を占め、一般的に肝硬変や慢性B型肝炎ウイルス患者に発生する早期肝細胞がん(HCC)を検出する優れた方法につながる可能性があります。この実験法は、細胞外小胞(EV)として知られるナノ粒子を分析・解析するもので、EVは正常細胞から放出されるが、特に腫瘍細胞や腫瘍微小環境内の細胞から放出されます。
さらに、UCLAの研究者とパートナーは、8つのHCC EV亜集団を分離して測定できる簡易表面タンパク質アッセイ(HCC EV SPA)を開発しました。科学者たちは、HCC EV SPA技術によって、リスクのある肝硬変患者の早期HCCを迅速、高感度、低コストで同定できる日が来るだろうと考えています。少量の血漿サンプルからHCC EVを精製する独自のクリックビーズと、HCC EVのサブポピュレーションを測定するマルチプレックス・リアルタイム免疫PCRです。
また、研究者らは、早期HCCを検出するための国際肝がん学会バイオマーカー開発ガイドラインに従い、第2相バイオマーカー研究を実施しました。したがって、早期発見により、医師や患者はより早く治療を開始することができ、生存率に大きな影響を及ぼすと考えられます。このように、上記の要因により、予測期間中、市場は牽引役となることが期待されます。
肝がんの有病率の増加が世界の肝がん診断市場の成長を牽引すると期待される
米国国立がん研究所のSurveillance, Epidemiology, and End Results(SEER)プログラムによると、米国では2023年に新たに41,210例の肝臓がんおよび肝内胆管がんと診断され、約29,380人が原発性成人肝がんで死亡すると予測されています。5年相対生存率はわずか21.6%です。
B型肝炎、C型肝炎、肝硬変の罹患は成人原発性肝がんの重大な危険因子です。肝がんは女性よりも男性に多く、アジア系・太平洋諸島系住民やアメリカ・インディアン/アラスカ先住民に多いです。したがって、肝がんの発生が増加していることから、早期発見の必要性が高まっています。したがって、上記の要因により、予測期間中、市場は拡大すると予想されます。
肝がん診断のための組織サンプル採取の課題が世界の肝がん診断市場の成長を妨げると予想される
小さな腫瘍は、画像検査ですぐに見えなかったり、健康診断で触診できなかったりするため、生検が難しくなる可能性があります。腫瘍が小さければ小さいほど、診断に十分な組織サンプルを採取するために生検をより正確に行わなければならないです。
肝生検では合併症が起こる可能性があるが、熟練した医師が行えば通常安全であると考えられています。しかし、肝臓には豊富な血液が供給されているため、生検中または生検後に出血する危険性があります。その他の潜在的なリスクとしては、感染症、近隣臓器への危害、胆汁漏出などがあります。問題が起こる可能性が高いため、それぞれの状況において、生検を行うことの危険性と利点を慎重に検討する必要があります。
したがって、上記の要因により、予測期間中、市場は低迷すると予想されます。
ロシア・ウクライナ紛争分析
現在進行中のロシアとウクライナの紛争は、深刻な影響を及ぼす地政学的問題です。病院、診断研究所、医療施設などのホスピタリティ・インフラは、紛争の影響を受けた地域で損害を被ったり、アクセス不能になったりする可能性があります。このような混乱は、画像技術、生検法、臨床検査などの肝臓がん診断サービスの利用可能性やアクセス性に影響を及ぼす可能性があります。
紛争によりサプライチェーンが遮断され、診断機器、画像診断薬、生検器具、検査試薬などの医療物資の入手性が低下する可能性があります。このような物資不足は、肝がん診断技術の遅延や制限を引き起こし、タイムリーで正確な診断に影響を及ぼす可能性があります。
さらに、戦争によって放射線科医、病理医、腫瘍専門医などのヘルスケア専門家やその他の医療従事者が転出する可能性もあります。このような専門知識の喪失は、被災地の肝臓がん診断能力にさらなる負担をかけ、おそらく発見と治療の遅れにつながる可能性があります。
したがって、上記の要因を考慮すると、肝がん診断市場は戦争の結果、中程度の影響を受けたと言えます。
COVID-19の影響分析:
COVID-19の流行は肝がん診断に影響を与えています。COVID-19は既存の慢性肝疾患を悪化させ、肝がんの管理を複雑にする可能性があります。パンデミックは、診断から治療戦略まで、肝がん患者の管理に大きな影響を与えています。COVID-19による検診プログラムの変更は、肝がん診断の遅れの原因となっています。ある調査では、参加施設の80.9%がパンデミックによる肝がん診断の遅れを報告しています。
対照的に、COVID-19パンデミックの際には、ヘルスケアシステムがもたらす課題に適応し、ウイルスへの曝露リスクを最小限に抑えるために、肝臓がん検診の代替方法が実施されました。遠隔医療は、パンデミックの間、遠隔ヘルスケアサービスを提供するために広く利用されてきました。バーチャル診察により、ヘルスケアプロバイダーは患者の症状を評価し、病歴を確認し、肝臓がん検診の指導を行うことができます。
さらに、リスク評価ツールは、肝臓がんを発症するリスクが高い患者を特定するのに役立ちます。これらのツールは、年齢、性別、基礎疾患である肝疾患、その他の危険因子などの因子を考慮したものです。ヘルスケアプロバイダーはこれらのツールを用いて、さらなるスクリーニングやサーベイランスの必要性を判断することができます。
目次
第1章 調査手法と調査範囲
第2章 定義と概要
第3章 エグゼクティブサマリー
第4章 市場力学
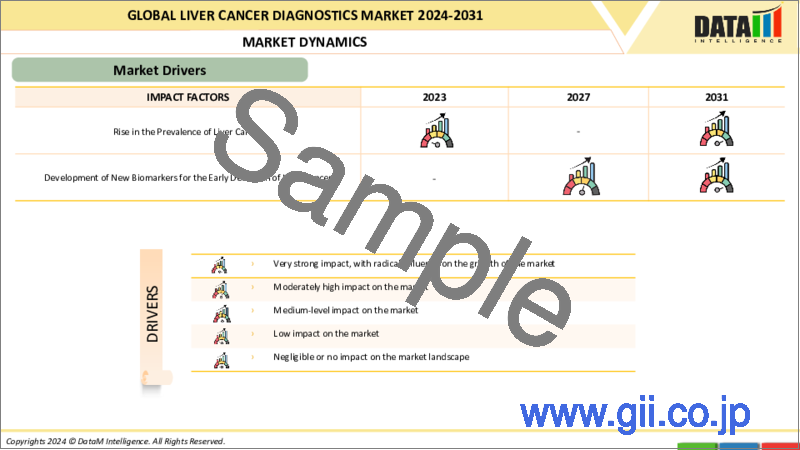
- 影響要因
- 促進要因
- 肝がんの早期発見のための市場参入企業による臨床試験の増加
- 肝がんの早期発見のための新しいバイオマーカーの開発
- 抑制要因
- 肝がんスクリーニングの高コスト
- 機会
- 肝がん診断におけるポイントオブケア検査(POCT)の需要の高まり
- 影響分析
- 促進要因
第5章 産業分析
- ポーターの5フォース分析
- サプライチェーン分析
- アンメットニーズ
- 規制分析
第6章 COVID-19分析
第7章 ロシア・ウクライナ戦争分析
第8章 検査タイプ別
- アルファフェトプロテイン(AFP)腫瘍マーカー検査
- 臨床検査
- バイオマーカー
- がん胎児抗原と糖タンパク質抗原
- 酵素とアイソ酵素
- 成長因子と受容体
- 分子マーカー
- 病理学的バイオマーカー
- 血液検査
- 肝機能検査(LFT)
- 血液凝固検査
- 腎機能検査
- 全血球計算(CBC)
- 血液化学検査およびその他の検査
- バイオマーカー
- 生検
- 細針吸引生検
- コア針生検
- 腹腔鏡検査
- 画像診断
- 超音波検査
- コンピュータ断層撮影(CT)
- 磁気共鳴画像法(MRI)
- 血管造影
- その他
- その他
第9章 エンドユーザー別
- 病院
- がん研究機関
- 診断研究所
- その他
第10章 地域別
- 北米
- 米国
- カナダ
- メキシコ
- 欧州
- ドイツ
- 英国
- フランス
- イタリア
- スペイン
- その他欧州
- 南米
- ブラジル
- アルゼンチン
- その他南米
- アジア太平洋
- 中国
- インド
- 日本
- オーストラリア
- その他アジア太平洋地域
- 中東・アフリカ
第11章 競合情勢
- 競合シナリオ
- 製品ベンチマーク
- 企業シェア分析
- 主な発展と戦略
第12章 企業プロファイル
- Abbott Laboratories
- 会社概要
- 製品ポートフォリオと説明
- 財務概要
- 主な発展
- F. Hoffmann-La Roche Ltd.
- Qiagen N.V.
- Thermo Fisher Scientific, Inc.
- Siemens Healthineers
- BD
- Illumina, Inc.
- Koninklijke Philips N.V
- Epigenomics AG
- Fujifilm Medical Systems U.S.A., Inc.
- Sysmex Corporation
第13章 付録
Market Overview
Global Liver Cancer Diagnostics Market reached US$ 8.6 billion in 2022 and is expected to reach US$ 14.1 billion by 2030 growing with a CAGR of 6.6% during the forecast period 2023-2030. Liver cancer is a malignant growth that starts in the liver and can spread to other parts of the body. It is one of the most common types of cancer worldwide. Early diagnosis is key to effectively treating liver cancer.
Currently, there are several diagnostic methods used to diagnose liver cancer. These include imaging tests, such as computed tomography (CT) scans and magnetic resonance imaging (MRI), as well as blood tests that measure levels of certain proteins and hormones. Biopsies can also be performed to collect cells for lab tests. Doctors can effectively detect liver cancer and establish an efficient treatment strategy if they understand the various diagnostic procedures available. Early diagnosis is critical for improving patient outcomes.
Furthermore, the increasing prevalence of liver cancer, rising approvals for novel liver cancer detection tests, and advancement in the imaging systems for liver cancer diagnosis are the factors expected to drive the market over the forecast period.
Market Dynamics
Technological Advancement in the Earlier Detection of Hepatocellular Carcinoma is Expected to Drive the Global Liver Cancer Diagnostics Market Growth
On August 4, 2022, According to new research led by UCLA Jonsson Comprehensive Cancer Centre investigators and involving more than 50 researchers, new technology in development may lead to a better way to detect early-stage hepatocellular carcinoma (HCC), which accounts for 80% to 85% of primary liver cancers and typically occurs in patients with liver cirrhosis or chronic hepatitis B virus. The experimental method analyses and analyses nanoparticles known as extracellular vesicles, or EVs, which are released by normal cells but especially by tumor cells and cells within a tumor microenvironment.
Additionally, UCLA researchers and partners developed a simplified surface protein assay (HCC EV SPA) capable of dissecting and measuring eight HCC EV subpopulations. The scientists believe that the HCC EV SPA technology will one day allow for the quick, highly sensitive, and low-cost identification of early-stage HCC in at-risk patients with liver cirrhosis. It is made up of two powerful platform technologies: proprietary Click Beads for purifying HCC EVs from small volumes of plasma samples, and multiplex, real-time immune-PCR for measurement of HCC EV subpopulations.
Also, the researchers have conducted a Phase 2 biomarker study, following the International Liver Cancer Association biomarker development guideline for detecting early-stage HCC. Therefore, early detection allows physicians and patients to begin therapy sooner, which they believe will have a major influence on survival rates. Thus, owing to the above factors, the market is expected to drive over the forecast period.
The Increasing Prevalence of Liver Cancer is Expected to Drive the Global Liver Cancer Diagnostics Market Growth
According to the National Cancer Institute's Surveillance, Epidemiology, and End Results (SEER), Program estimates that 41,210 new cases of liver and intrahepatic bile duct cancer will be diagnosed in the United States in 2023, with some 29,380 people expected to die of primary adult liver cancer. The five-year relative survival rate is just 21.6 percent.
Having hepatitis B, hepatitis C, or cirrhosis are significant risk factors for adult primary liver cancer. Liver cancer is more common in men than women and among Asian/Pacific Islander and American Indian/Alaska Native populations. Therefore, the rising occurrence of liver cancer raises the need for early detection. Thus, owing to the above factors, the market is expected to drive over the forecast period.
Challenges for Obtaining a Tissue Sample for Liver Cancer Diagnosis is Expected to Hamper the Global Liver Cancer Diagnostics Market Growth
Small tumors can be more difficult to biopsy since they may not be immediately visible on imaging investigations or palpable during a physical examination. The smaller the tumor, the more exact the biopsy must be to acquire a sufficient tissue sample for diagnosis.
Complications are possible with liver biopsy procedures, however, they are typically regarded as safe when performed by skilled physicians. However, due to the liver's abundant blood supply, there is a danger of bleeding during or after the biopsy. Other potential risks include infection, harm to neighboring organs, and bile leakage. The likelihood of problems necessitates careful consideration of the dangers vs the advantages of performing a biopsy in each situation.
Thus, owing to the above factors, the market is expected to hamper over the forecast period.
Russia-Ukraine Conflict Analysis
The ongoing conflict between Russia and Ukraine is a geopolitical issue with profound ramifications. Healthcare infrastructure, such as hospitals, diagnostic laboratories, and medical facilities, may suffer damage or be rendered inaccessible in conflict-affected areas. This disruption may affect the availability and accessibility of liver cancer diagnostic services such as imaging technologies, biopsy procedures, and laboratory tests.
Conflicts may interrupt supply chains and reduce the availability of medical supplies such as diagnostic equipment, imaging agents, biopsy tools, and laboratory reagents. This scarcity can cause delays or limits in liver cancer diagnostic techniques, affecting timely and accurate diagnosis.
In addition, the war may cause the displacement of healthcare experts such as radiologists, pathologists, and specialized oncologists, as well as other medical personnel. This loss of expertise may place a further strain on the afflicted regions' liver cancer diagnostic capabilities, perhaps leading to delays in detection and treatment.
Therefore, taking into account the factors mentioned above, it can be stated that the liver cancer diagnostic market experienced a moderate impact as a result of the war.
COVID-19 Impact Analysis:
The COVID-19 pandemic has had an impact on liver cancer diagnosis. COVID-19 can exacerbate existing chronic liver disease and complicate the management of liver cancer. The pandemic has significantly impacted the management of liver cancer patients, from diagnosis to treatment strategies. The modification of screening programs due to COVID-19 has caused delays in liver cancer diagnosis. In a study, 80.9% of participating centers reported a delay in liver cancer diagnosis due to the pandemic.
In contrast, during the COVID-19 pandemic, alternative methods for liver cancer screening have been implemented to adapt to the challenges posed by the healthcare system and to minimize the risk of exposure to the virus. Telemedicine has been widely used during the pandemic to provide remote healthcare services. Virtual consultations allow healthcare providers to assess patients' symptoms, review medical history, and provide guidance on liver cancer screening.
Additionally, risk assessment tools can help identify individuals who are at a higher risk of developing liver cancer. These tools take into account factors such as age, gender, underlying liver disease, and other risk factors. Healthcare providers can use these tools to determine the need for further screening or surveillance.
Segment Analysis
The global liver cancer diagnostics market is segmented based on test type, end user, and region.
Hospitals from the End User Segment Account for 35.52% of the Market Share Owing to the Advanced Imaging Technologies, Integration of Test Results, Increased Diagnostic Testing Demand, and Increasing Number of Hospitals with Imaging Modalities and Screening Facilities.
Hospitals play a vital role in cancer diagnosis, with numerous advantages leading to precise diagnosis and appropriate disease management.
The hospital is equipped with cutting-edge imaging equipment such as computed tomography (CT), magnetic resonance imaging (MRI), and positron emission tomography (PET) scanners.
These cutting-edge diagnostic tests provide detailed, fascinating images of the liver to aid in the diagnosis, characterization, and staging of liver tumors. Specialized tests, such as CT angiography or diffusion-weighted imaging, may be performed in clinical laboratories to examine vascular involvement or detect subtle changes in the tumor.
For instance, Cancer Treatment Centers of America (CTCA) is now the City of Hope, joining forces to expand patient access to personalized, comprehensive cancer care. Moreover, the City of Hope is committed to providing the highest level of care for patients experiencing liver cancer and other gastrointestinal malignancies.
Thus, owing to the above factors, the market segment is expected to hold the largest market share over the forecast period.
Geographical Analysis
North America Accounted for Approximately 39.6% of the Market Share Owing to the Rising Implementation of Novel Diagnostics, the Presence of Supportive Government Organizations, and Collaborations among Market Players
According to National Center for Biotechnology Information Article 2022, Texas has the highest age-adjusted incidence rate of hepatocellular carcinoma (HCC) in the United States. To address cancer prevention and early detection through research, the Cancer Prevention and Research Institute of Texas (CPRIT) has funded the Texas Collaborative Center for Hepatocellular Cancer (TeCH) to facilitate liver cancer research, education, and advocacy activities. TeCH and its committees facilitate connections and collaborations among HCC researchers and clinicians, healthcare leaders, biotechnology companies, and the public to reduce liver cancer mortality in Texas by 2030.
Additionally, on December 8, 2022, the Department of Veterans Affairs (VA) will research to discover the most efficient screening technique for liver cancer, a lethal malignancy that can be cured if detected early. This is the largest clinical experiment in the history of liver cancer screening. The trial will look into whether finding liver cancer early using a shortened MRI reduces patients' chance of death.
PREMIUM - PREventing Liver Cancer Mortality via Imaging with Ultrasound vs. MRI - the trial's goal is to evaluate whether screening using shortened MRI is better than ultrasound, the current standard of care, in lowering liver cancer fatalities in veterans. VA's Veterans Health Administration is the largest healthcare provider in the U.S. for patients with cirrhosis, a leading risk factor for liver cancer.
Enrollment will begin in 2023 and follow participants over eight years. This is the first clinical trial to compare the two screening methods for their effect on patient outcomes. Thus, owing to the above factors, the North American region is expected to hold the largest market share over the forecast period.
Competitive Landscape
The major global players in the market include: Abbott Laboratories, F. Hoffmann-La Roche Ltd., Qiagen N.V., Thermo Fisher Scientific, Inc., Siemens Healthineers, BD, Illumina, Inc., Koninklijke Philips N.V, Epigenomics AG, Fujifilm Medical Systems U.S.A., Inc., and Sysmex Corporation among others.
Why Purchase the Report?
- To visualize the global liver cancer diagnostics market segmentation based on the test type, end user, and region, as well as understand key commercial assets and players.
- Identify commercial opportunities by analyzing trends and co-development.
- Excel data sheet with numerous data points of liver cancer diagnostics market-level with all segments.
- PDF report consists of a comprehensive analysis after exhaustive qualitative interviews and an in-depth study.
- Product mapping available as Excel consisting of key products of all the major players.
The global liver cancer diagnostics market report would provide approximately 53 tables, 50 figures, and 195 Pages.
Target Audience 2023
- Manufacturers/ Buyers
- Industry Investors/Investment Bankers
- Research Professionals
- Emerging Companies
Table of Contents
1. Methodology and Scope
- 1.1. Research Methodology
- 1.2. Research Objective and Scope of the Report
2. Definition and Overview
3. Executive Summary
- 3.1. Snippet by Test Type
- 3.2. Snippet by End User
- 3.3. Snippet by Region
4. Dynamics
- 4.1. Impacting Factors
- 4.1.1. Drivers
- 4.1.1.1. Increasing Clinical Trials by the Market Players for the Early Detection of Liver Cancer
- 4.1.1.2. Development of New Biomarkers for the Early Detection of Liver Cancer
- 4.1.2. Restraints
- 4.1.2.1. The High Cost of Liver Cancer Screening
- 4.1.3. Opportunity
- 4.1.3.1. Rising Demand for Point-Of-Care Testing (POCT) in Liver Cancer Diagnostics
- 4.1.4. Impact Analysis
- 4.1.1. Drivers
5. Industry Analysis
- 5.1. Porter's 5 Forces Analysis
- 5.2. Supply Chain Analysis
- 5.3. Unmet Needs
- 5.4. Regulatory Analysis
6. COVID-19 Analysis
- 6.1. Analysis of COVID-19
- 6.1.1. Scenario Before COVID-19
- 6.1.2. Scenario During COVID-19
- 6.1.3. Scenario Post COVID-19
- 6.2. Pricing Dynamics Amid COVID-19
- 6.3. Demand-Supply Spectrum
- 6.4. Government Initiatives Related to the Market During the Pandemic
- 6.5. Manufacturers' Strategic Initiatives
- 6.6. Conclusion
7. Russia-Ukraine War Analysis
8. By Test Type
- 8.1. Introduction
- 8.1.1. Market Size Analysis and Y-o-Y Growth Analysis (%), By Test Type
- 8.1.2. Market Attractiveness Index, By Test Type
- 8.2. Alpha-fetoprotein (AFP) tumor marker test*
- 8.2.1. Introduction
- 8.2.2. Market Size Analysis and Y-o-Y Growth Analysis (%)
- 8.3. Laboratory Tests
- 8.3.1. Biomarker
- 8.3.1.1. Oncofetal and Glycoprotein Antigens
- 8.3.1.2. Enzymes and Isoenzymes
- 8.3.1.3. Growth Factors and Receptors
- 8.3.1.4. Molecular Markers
- 8.3.1.5. Pathological Biomarkers
- 8.3.2. Blood Tests
- 8.3.2.1. Liver function tests (LFTs)
- 8.3.2.2. Blood clotting tests
- 8.3.2.3. Kidney function tests
- 8.3.2.4. Complete blood count (CBC)
- 8.3.2.5. Blood chemistry tests and other tests
- 8.3.1. Biomarker
- 8.4. Biopsy
- 8.4.1. Fine-needle aspiration biopsy
- 8.4.2. Core needle biopsy
- 8.4.3. Laparoscopy
- 8.5. Imaging
- 8.5.1. Ultrasound
- 8.5.2. Computed tomography (CT)
- 8.5.3. Magnetic resonance imaging (MRI)
- 8.5.4. Angiography
- 8.5.5. Others
- 8.6. Others
9. By End User
- 9.1. Introduction
- 9.1.1. Market Size Analysis and Y-o-Y Growth Analysis (%), By End User
- 9.1.2. Market Attractiveness Index, By End User
- 9.2. Hospitals*
- 9.2.1. Introduction
- 9.2.2. Market Size Analysis and Y-o-Y Growth Analysis (%)
- 9.3. Cancer Research Institutes
- 9.4. Diagnostic Laboratories
- 9.5. Others
10. By Region
- 10.1. Introduction
- 10.1.1. Market Size Analysis and Y-o-Y Growth Analysis (%), By Region
- 10.1.2. Market Attractiveness Index, By Region
- 10.2. North America
- 10.2.1. Introduction
- 10.2.2. Key Region-Specific Dynamics
- 10.2.3. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Test Type
- 10.2.4. Market Size Analysis, and Y-o-Y Growth Analysis (%), By End User
- 10.2.5. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Country
- 10.2.5.1. U.S.
- 10.2.5.2. Canada
- 10.2.5.3. Mexico
- 10.3. Europe
- 10.3.1. Introduction
- 10.3.2. Key Region-Specific Dynamics
- 10.3.3. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Test Type
- 10.3.4. Market Size Analysis, and Y-o-Y Growth Analysis (%), By End User
- 10.3.5. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Country
- 10.3.5.1. Germany
- 10.3.5.2. U.K.
- 10.3.5.3. France
- 10.3.5.4. Italy
- 10.3.5.5. Spain
- 10.3.5.6. Rest of Europe
- 10.4. South America
- 10.4.1. Introduction
- 10.4.2. Key Region-Specific Dynamics
- 10.4.3. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Test Type
- 10.4.4. Market Size Analysis, and Y-o-Y Growth Analysis (%), By End User
- 10.4.5. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Country
- 10.4.5.1. Brazil
- 10.4.5.2. Argentina
- 10.4.5.3. Rest of South America
- 10.5. Asia Pacific
- 10.5.1. Introduction
- 10.5.2. Key Region-Specific Dynamics
- 10.5.3. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Test Type
- 10.5.4. Market Size Analysis, and Y-o-Y Growth Analysis (%), By End User
- 10.5.5. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Country
- 10.5.5.1. China
- 10.5.5.2. India
- 10.5.5.3. Japan
- 10.5.5.4. Australia
- 10.5.5.5. Rest of Asia Pacific
- 10.6. Middle East and Africa
- 10.6.1. Introduction
- 10.6.2. Key Region-Specific Dynamics
- 10.6.3. Market Size Analysis, and Y-o-Y Growth Analysis (%), By Test Type
- 10.6.4. Market Size Analysis, and Y-o-Y Growth Analysis (%), By End User
11. Competitive Landscape
- 11.1. Competitive Scenario
- 11.2. Product Benchmarking
- 11.3. Company Share Analysis
- 11.4. Key Developments and Strategies
12. Company Profiles
- 12.1. Abbott Laboratories*
- 12.1.1. Company Overview
- 12.1.2. Product Portfolio and Description
- 12.1.3. Financial Overview
- 12.1.4. Key Developments
- 12.2. F. Hoffmann-La Roche Ltd.
- 12.3. Qiagen N.V.
- 12.4. Thermo Fisher Scientific, Inc.
- 12.5. Siemens Healthineers
- 12.6. BD
- 12.7. Illumina, Inc.
- 12.8. Koninklijke Philips N.V
- 12.9. Epigenomics AG
- 12.10. Fujifilm Medical Systems U.S.A., Inc.
- 12.11. Sysmex Corporation
LIST NOT EXHAUSTIVE
13. Appendix
- 13.1. About Us and Services
- 13.2. Contact Us